Tel:
Fax:
Email:

www.hayatiboskut.com.tr

















Yörünge Enerjisi
Potansiyel enerji Ep ise; elektronu bulunduğu yörüngeden alıp sonsuza götürmek için gereken enerjinin ters işaretlisine eşittir.
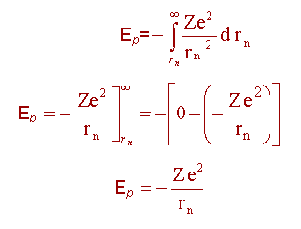
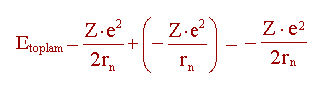
Elektronun toplam enerjisi için, Etoplam = Ek+Ep olduğuna göre Etoplam bulunmuş olur.
Bir kaç adım önce bulmuş olduğumuz rn değerini son bulduğumuz bağıntıda da yerine koyarsak; n sayılı yörünge için enerji bağıntısını bulmuş olacağız.
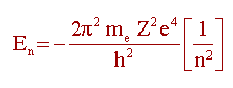
Denklemde me = 9,1.10-
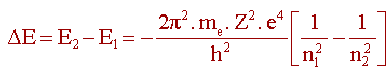
En (iki denklem önce bulunan) eşitliği, elektronun atomda n yörünge sayısına bağlı olarak yalnız belirli enerji seviyelerinde bulunabileceğini gösterir. Bu, kuantum hipotezinin temel alınmasının sonucudur. Serbest elektronların enerjisi bu modelde 0 (sıfır) kabul edildiği için, ondan daha az enerjisi olan atomdaki yörünge elektronların enerjisi negatiftir. En düşük enerji düzeyi; n = 1 yörüngesindedir ve n’nin değeri arttıkça enerji değeri sıfıra yaklaşarak büyür, n = 'da E = 0'dır. Bu halde elektron atomdan tamamen ayrılmıştır. İyonlaşmış atom veya pozitif iyon meydana gelir.
2.3.9 Broglie Varsayımının Tartışılması
h/ = m eşitliğine göre bir cismin kütlesi ve bazı arttıkça dalga boyu küçülmektedir. Bu yüzden kalem, top, otomobil gibi makroskopik cisimlerin dalga hareketi gözlenemez. Örneğin 600 g’lık bir futbol topunun ışık hızıyla hareket ettiğini varsayalım. Top dalga hareketi yapacak olursa dalga boyu 3,68 10-
* İşlemleri görmek için tıklayınız.
Bu değer bilinen en küçük büyüklüklerden, örneğin çekirdek çapından (~10–12 cm) 1028 kat daha küçüktür. Bu büyüklük bilinen fizik imkânlar dahilinde hiçbir şekilde ölçülemez, tespit edilemez ve bu yüzden bir fizik anlam taşımaz. Esasen Broglie’nin varsayımı, mikro ölçülerdeki elektron ve proton gibi atomik cisimler ve foton içindir.
Elektronlardan ibaret bir ışın demetinin kristalden yansırken dalga özelliklerinin ortaya çıkması 1927’de Broglie’nin teorisini ileri sürmesinden 3 yıl sonra denel olarak gözlenmiştir. Mikro ölçülerde de olsa bir cismin hem dalga hem de tanecik özelliğine sahip olması ilk anda bir çelişki olarak görülebilir. Ancak, dalga-
2.3.10 Heisenberg Belirsizlik İlkesi
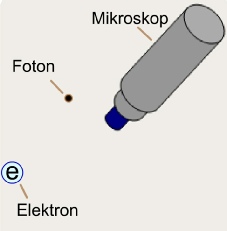
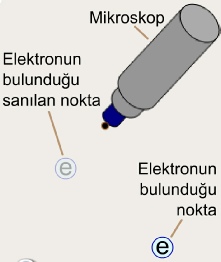
Bohr ve diğer atom modellerinin yetersiz oluşlarının ana sebeplerinden ikincisi elektronun atomdaki yerini ve davranış biçimini doğru olarak tarif edememeleridir. Konuyla ilgili modern fikirler Heisenberg tarafından ileri sürülmüştür.
Bu görüşe göre; elektronun atomdaki yerini ve hızını (veya hızından kaynaklanan momentumunu) aynı anda bilmek imkânsızdır. Başka bir ifade ile; elektronun yeri ve hızı ne teorik ne de denel yolla aynı anda tam olarak belirlenemez.
Özetle; elektronun hızı o kadar belirsizdir ki bu yüzden bir yörüngeyi belirtmeye imkân yoktur. Bohr Atom Modeli'nde önerilen kesin elektron yörüngelerinin hiçbir anlamı yoktur. Belirsizlik İlkesi'ne göre yapılan bu açıklamalar varsayılan bir deneyi anlattığı için aynı zamanda yörüngelerin varlığının denel yollarla da hiçbir zaman ispatlanamayacağını gösterir. Böylece, Bohr ve modifiye Bohr Tipi Atom Modellerini yetersiz kılan ikinci temel sebep ortaya çıkar.
2.3.11 Schrödinger Dalga Denklemi
De Broglie Bağıntısı, serbestçe hareket eden mikro cisimlerin davranışlarındaki tanecik ve dalga özelliklerini belirlemede temel olmuştur. Erwin Schrödinger, bu düşünce ortaya atıldıktan kısa bir süre sonra, de Broglie bağıntısının, atomdaki elektronlar gibi birbirlerine bağlı taneciklere uygulanmak üzere genelleştirilebileceğini göstermiştir.
Modern Atom Bilgisi'ne başlangıç yapan Schrödinger Teorisi, fiziksel sistemlerin mümkün olabilen enerjilerinin, klasik dalga teorisindeki eşitliklere çok benzeyen bir denklemi çözerek bulunabilmesi varsayımına dayanır. Bu düşünceye de; Broglie’nin teorik yaklaşımının yanı sıra, elektron akısı altındaki kristalleri gözleyerek elektronun dalga hareketini denel olarak ispatlayan Davisson ve Germer’in denel başarısı, önemli ölçüde destek olmuştur.
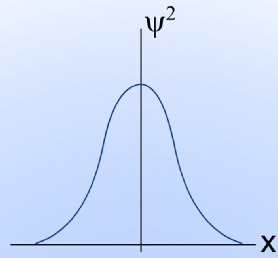
Atomdaki elektronları üç boyutlu dalga hareketi yapan tanecikler olarak kabul eden Schrödinger, kendi adı ile anılan dalga denklemini, titreşen bir noktanın dalga hareketini tanımlayarak türetmiştir.

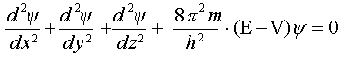
2.3.12 Dalga Denklemi ve Fiziksel Gerçeklik
Matematik fonksiyonların çözümünden elde edilen sonuçların hepsinin fiziksel anlam taşıması beklenmez. Bu nedenle sistemin fizik anlamı olan ve gözlenebilen özelliklerinden birini elde edebilmek için, fonksiyonlara sınırlayıcı varsayımlar getirilmesine ihtiyaç vardır. Bu amaçla, dalga mekaniği kapsamında elektronun davranışını açıklayabilmek için üç varsayım geliştirilmiştir.
1-
Kararlı atomik sistemlerin incelenmesinde zamandan bağımsız fonksiyonlar kullanılır.
2-
3-
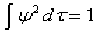
 Genel Kİmya konlarI
Genel Kİmya konlarI Gerİ
Genel Kİmya konlarI Devam
Genel Kİmya konlarI
Genel Kİmya konlarI Gerİ
Genel Kİmya konlarI Devam