




Tel:
Fax:
Email:

www.hayatiboskut.com.tr

















3.4.6.1 Asal Gazlar
Helyum havadan hafif ve yanmayan bir gazdır, meteoroloji balonlarında kullanılır. Argon, havaya karşı duyarlı maddelerin korunması için, metallere kaynak yapılması sırasında yükseltgenmeyi engellemek için koruyucu gaz olarak kullanılır. Ayrıca asal gazlar neon lambaları, fluoresan lambaları gibi çeşitli aydınlatma araçlarında kullanılır. Helyum, başta Neon olmak üzere lazer ışınlarının eldesinde kullanılır.
1962 yılına kadar, asalgaz bileşiklerinin elde edilmesiyle ilgili çalışmalar başarılı olmamıştır. Asal gazların ayrıca 3C6H4(OH)2. 0,7 Kr gibi bazı katıların bileşiminde olduğu belirlenmiştir. Ancak bu bileşikler gerçek asal gaz bileşikleri değildir. Katı oluşumunda bazı moleküllerin arasında kalan uygun büyüklükteki boşluklara asal gazların yerleşmesiyle oluşmuşlardır. Böyle bileşiklere kafes bileşikler denir.
İlk Ksenon bileşiği 1962'de Neil Bartlett tarafından ksenonun PtF6 ile reaksiyonu ile Xe(PtF6) bileşiği şeklinde izole edilmiştir. Bartlett, platin hekzafluorür ile yapmakta olduğu deneyler sırasında O2(PtF6) bileşiğini oluşturmuştur. O2 'nin iyonlaşma enerjisi ile Xe'nin iyonlaşma enerjilerinin birbirine yakın olduğunu düşünen Bartlett, ilk asalgaz bileşiğinin sentezini yapabilmiştir.
Bugün ksenonun fluor bileşikleri nikelden yapılmış reaksiyon kaplarında elementel haldeki ksenon ve fluorun doğrudan reaksiyonu ile yapılmaktadır. Kapların iç yüzü NiF2 ile kaplanarak fluorun kap ile etkileşmesi önlenmektedir. Değişen sıcaklık ve basınç şartlarında XeF2, XeF4 ve XeF6 bileşikleri elde edilebilmektedir. Ksenonun diğer bileşiklerinin çoğu fluorürlerinin hidrolizi sonucunda oluşurlar.

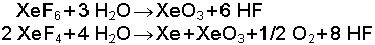
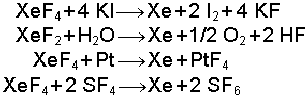
Suyun aşırı olması halinde ksenon oksit oluşur.
Ksenon fluorürlerin hepsi yükseltgen bileşiklerdir ve fluorür vericileri olarak davranırlar. Reaksiyonlarında elementel ksenon ve yükseltgenme ürünleri verirler.
Radon ksenondan daha düşük iyonlaşma enerjisine sahiptir ve kimyasal reaksiyonlara daha yatkındır. RnF2 ve benzer bileşikleri oluşturabilir. Ancak radonun radyoaktif olması nedeniyle bu bileşiklerin yapılarının ve özelliklerinin belirlenmesi güçtür. Doğaya saldığı ışımaların şiddeti, kozmik ışınların ve diğer ışımaların oluşturduğu doğal ışıma düzeyinin üstünde değildir. Ancak önemli ölçüde uranyum içeren kayalardan hazırlanan yapı malzemelerinde normal sınırların üzerinde radon çıkışı gözlenmiştir.
Kripton çok daha büyük iyonlaşma enerjisi nedeniyle oluşturduğu bileşiklerin sayısı çok daha sınırlıdır. Kripton difluorür (KrF2), düşük sıcaklıklarda (-
Bölüm Özeti
Atomun Yapısı bölümünü tamamladınız. Bu bölümde anlatılan konular kısaca şöyledir;
Elementlerin belirli bir kurala göre dizilmesi ilk defa Döbereiner tarafından 1817 yılında Triadlar Kuralı olarak öne sürülmüştür. 1863 yılında John Newlands ise Oktav Kuralı ile sistematik bir düzenlemeye ilk adımı atmıştır. Modern periyodik cetvel 1868-